En una primicia mundial que desafía lo que creíamos saber sobre biología, un equipo de científicos han logrado crear células animales capaces de realizar la fotosíntesis. El avance promete revolucionar la investigación médica y aumentar la producción de carne cultivada en laboratorio.
La fotosíntesis es un proceso bioquímico que utilizan las plantas, las algas y ciertas bacterias para convertir la energía luminosa del sol en alimento. El proceso -que tiene lugar en unas estructuras celulares especiales llamadas cloroplastos- consume agua y dióxido de carbono y produce oxígeno, así como azúcares que pueden ser utilizados por la planta.
Sachihiro Matsunaga, profesor del Laboratorio de Biología Integrada de la University of Tokyo que dirigió la investigación, dijo en un comunicado:
“Todos los organismos vivos de la Tierra, incluidos los humanos, pueden vivir gracias a la fotosíntesis. Las células animales consumen oxígeno, comen y descomponen azúcares y emiten dióxido de carbono. Esta reacción es completamente opuesta a la fotosíntesis”.
Los científicos llevan desde la década de 1970 intentando que se produzca la fotosíntesis en los animales.
Matsunaga afirma:
“Si conseguimos que se produzca aunque sólo sea una parte de la fotosíntesis en las células animales, podremos reducir la cantidad de oxígeno consumido, reducir la cantidad de azúcar consumido y reducir las emisiones de dióxido de carbono”.
Sin embargo, insertar estos cloroplastos en células animales es mucho más fácil de decir que de hacer.
Cloroplastos que funcionan en una célula animal
Matsunaga explicó:
“Las células animales reconocen los cloroplastos como extraños y los destruyen de inmediato, por lo que los cloroplastos no funcionaron ni siquiera cuando se introdujeron en células animales. Como resultado, al cabo de unos 10 años, todo el mundo dejó de investigar. Se convirtió en ‘conocimiento común’ en el campo biológico que los cloroplastos por sí mismos no funcionan en células animales.”
Además de parecer un material “extraño”, los cloroplastos luchan por funcionar en el entorno de una célula animal.
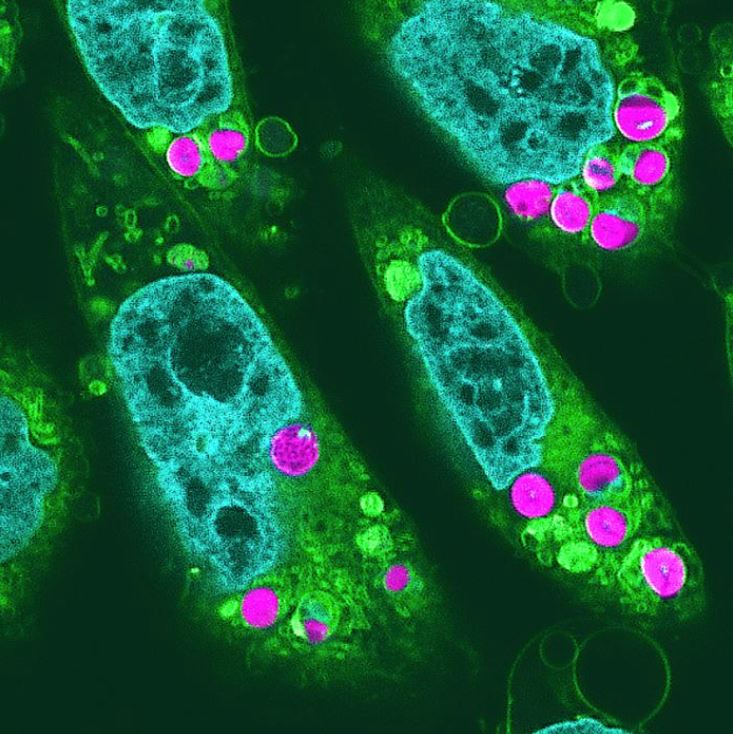
Esta imagen de fluorescencia muestra cloroplastos (de color magenta) incorporados con éxito a las células de hámster, con otras características de la célula animal también resaltadas (núcleos en azul claro y orgánulos en amarillo-verde). Crédito de imagen: R. Aoki, Y. Inui, Y. Okabe et al. 2024/ Proceedings of the Japan Academy, Series B
Matsunaga explica:
“Casi todas las algas y especies vegetales realizan la fotosíntesis por debajo de los 30 grados centígrados. La mayoría de las células animales se cultivan a 37 grados centígrados”.
Por tanto, los investigadores tuvieron que buscar cloroplastos capaces de funcionar en el ambiente cálido de una célula animal.
Matsunaga dijo:
“El éxito de este estudio se atribuye al aislamiento de cloroplastos de schyzon, que crece en una fuente termal volcánica de Italia a 42 grados Celsius y tiene actividad cloroplástica incluso a 37 grados Celsius”.
El siguiente paso fue impedir que las células animales rechazaran los cloroplastos como material “extraño”.
Matsunaga explica:
“Cuando los cloroplastos se introducen a la fuerza en las células animales, se reconocen como sustancias extrañas, como bacterias o virus, y se degradan rápidamente. [Sin embargo, nuestros] cloroplastos se administraron a células animales como alimento, en lugar de introducirlos a la fuerza en células animales.
Los cloroplastos ingeridos como alimento pudieron mantenerse en la célula animal durante al menos dos días, tiempo durante el cual pudo detectarse la reacción inicial de fotosíntesis. Es la primera vez en el mundo que hemos podido detectar la reacción inicial de fotosíntesis en células animales. Hemos sido capaces de dar un vuelco al sentido común en biología”.
Células animales con cloroplastos mostraron mayor tasa de crecimiento
Representación digital de una célula híbrido animal-planta. Crédito de imagen: DALL-E / codigooculto.com
No sólo eso, las células animales que contenían cloroplastos mostraron una mayor tasa de crecimiento, lo que sugiere que los cloroplastos estaban proporcionando una fuente alternativa de alimento a sus huéspedes.
Matsunaga dijo:
“Me sorprendió porque fuimos capaces de hacer algo que nadie había sido capaz de hacer durante 50 años y que todos los investigadores biológicos habían dado por perdido”.
Entonces, ¿significa esto que todos podremos empezar a hacer la fotosíntesis? Todavía no.
Matsunaga dijo:
“Dado que nuestra tecnología está adaptada a células animales cultivadas, el camino más corto es considerarla útil para el desarrollo de [mini órganos modelo para investigación médica] y carne artificial. Cuando las células se vuelven multicapa, el interior de la masa celular [no recibe suficiente oxígeno,] la división celular se detiene y no es posible aumentar de tamaño. Sin embargo, si la luz puede llegar al interior de la masa celular, los cloroplastos capturados pueden suministrar oxígeno, la condición [de poco oxígeno] en el interior de la masa celular puede mejorar y la división celular puede reanudarse.”
En el futuro, este proceso también puede resultar prometedor en entornos médicos, por ejemplo si los pacientes necesitan que se suministre más oxígeno a determinados órganos.
Matsunaga explicó:
“Si el objetivo de la terapia es repartir oxígeno cerca de los vasos sanguíneos del corazón para mejorar las cardiopatías, bastaría con implantar una fuente de luz LED cerca del corazón”.
Sin embargo, antes de que eso ocurra, el equipo tendrá que mantener los cloroplastos en funcionamiento durante más de dos días, como ocurrió en este experimento.
Matsunaga afirma:
“En el futuro, mejoraremos nuestra técnica para que los cloroplastos puedan realizar la fotosíntesis en células animales durante el mayor tiempo posible”.
Los hallazgos de la investigación titulada “Incorporation of photosynthetically active algal chloroplasts in cultured mammalian cells towards photosynthesis in animals” han sido publicados en Proceedings of the Japan Academy Series B.
[FT: eurekalert]
¿Te gustó este contenido? Te invito a compartirlo con tus amigos. Síguenos en nuestra Página de Facebook, para recibir a diario nuestras noticias. También puedes unirte a nuestro Grupo Oficial y a nuestra comunidad en Telegram.








0 comentarios